Trotz jahrzehntelanger Fortschritte folgt die Krebsbehandlung nach wie vor demselben Muster: Ärzte greifen erst ein, wenn die Krankheit bereits fortgeschritten ist. Zu diesem Zeitpunkt haben Krebszellen gelernt zu überleben, dem Immunsystem zu entgehen und sich mitunter in andere Körperteile auszubreiten. Krebs von vornherein zu verhindern wäre in der Regel einfacher als ihn zu behandeln. Ein neuer Ansatz mit einem rekombinanten Proteinimpfstoff will dieses Paradigma verändern, indem er das Immunsystem darauf trainiert, α-Lactalbumin zu erkennen – ein Protein, das in vielen Fällen von dreifach negativem Brustkrebs (TNBC) vorkommt. Erste klinische Studien mit dieser Strategie haben vielversprechende Ergebnisse gezeigt und geben Hoffnung, eine der aggressivsten und am schwersten zu behandelnden Formen von Brustkrebs zu verhindern.
Die Bedrohung durch dreifach negativen Brustkrebs (TNBC)
Im Jahr 2021, mit 31 Jahren, bemerkte Chase Johnson etwas Ungewöhnliches. Ihr Hund war ungewöhnlich unruhig geworden und klammerte sich ständig an sie. Eines Tages drückte er seine Nase fest gegen ihre Brust. Johnson ertastete einen harten Knoten und wusste, dass etwas nicht stimmte. Sie ging daraufhin zum Arzt und erhielt leider die Diagnose dreifach negativer Brustkrebs (TNBC), eine Form von Brustkrebs, die häufig jüngere Frauen betrifft und aggressiver verläuft. Nach monatelanger intensiver Behandlung mit intravenöser Chemotherapie und Operation, gefolgt von zusätzlicher oraler Chemotherapie und Strahlentherapie, wurde Johnson für krebsfrei erklärt.
Wäre es ein häufiger, hormonrezeptorpositiver Brustkrebs gewesen, wären die Langzeitaussichten für Johnson beruhigender gewesen. Doch TNBC birgt ein anderes Risikoprofil. Die Wahrscheinlichkeit eines metastasierten Rezidivs ist um ein Vielfaches höher. Selbst nach erfolgreicher Behandlung erleiden etwa 40 % der Patientinnen innerhalb von fünf Jahren einen Rückfall. In diesen Fällen handelt es sich häufig um einen metastasierten Rückfall, der entfernte Organe wie Gehirn, Lunge oder Leber befällt – Bereiche, in denen die Therapieoptionen begrenzter und die klinischen Ergebnisse schlechter sind. Erschwerend kommt hinzu, dass es derzeit keinen standardisierten klinischen Test gibt, der das Rezidivrisiko bei TNBC-Überlebenden zuverlässig vorhersagen kann.
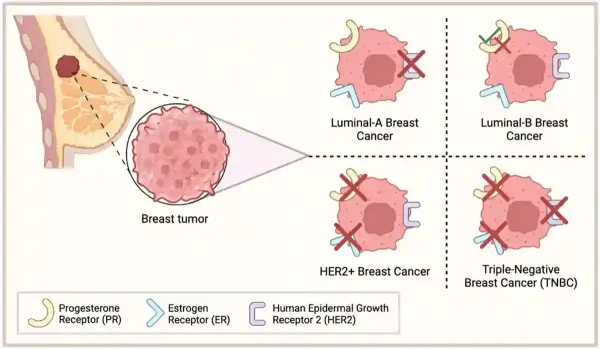
Noch schlimmer ist, dass TNBC etwa 15 % aller Brustkrebsfälle ausmacht und bekanntermaßen schwer zu behandeln ist. Per Definition bedeutet „dreifach negativ“ bei TNBC, dass drei molekulare Zielstrukturen fehlen, die den meisten modernen Brustkrebstherapien zugrunde liegen: der Östrogenrezeptor, der Progesteronrezeptor und der humane epidermale Wachstumsfaktorrezeptor 2 (HER2) (Abbildung 1). Ohne diese Zielstrukturen sind Standard-Hormontherapien und HER2-gerichtete Medikamente wirkungslos. Die Chemotherapie bleibt die wichtigste Behandlungsoption, trägt aber kaum dazu bei, ein Wiederauftreten des Krebses zu verhindern. Ohne diese Zielstrukturen sind Standard-Hormontherapien und auf den HER2-Rezeptor gerichtete Medikamente wirkungslos.
Für Patientinnen wie Johnson, die bereits intensive Therapien durchlaufen haben und sogar als krebsfrei galten, bedeutet das verbleibende Rückfallrisiko eine lange Zeit der Ungewissheit. Genau dieses anhaltende Risiko veranlasste Johnson, an einer klinischen Studie der frühen Phase teilzunehmen, in der eine neuartige rekombinante Proteinimpfstoffstrategie für TNBC getestet wurde. Der Impfstoff soll das Immunsystem trainieren, α-Lactalbumin zu erkennen, ein Protein, das in vielen TNBC-Zellen abnormal exprimiert wird. Dadurch soll der Impfstoff ein Wiederauftreten der Erkrankung verhindern und bei Hochrisikopatientinnen die Entstehung von TNBC von vornherein verhindern.
Abbildung 1. Klassifizierung von Brustkrebs anhand von Oberflächenmarkern. Brustkrebs wird danach eingeteilt, ob seine Zellen Östrogenrezeptoren, Progesteronrezeptoren und/oder den humanen epidermalen Wachstumsfaktorrezeptor 2 (HER2) exprimieren. Luminale Tumoren weisen einen oder mehrere Hormonrezeptoren auf, HER2-positive Tumoren sind auf den HER2-Switch angewiesen, und dreifach negativer Brustkrebs (TNBC) besitzt keinen der drei Rezeptoren. Quelle: Kirkby et al. (2023), Cancers.
α-Lactalbumin-Impfstoff gegen TNBC: Die Begründung
Das Besondere an diesem Impfstoffkonzept gegen dreifach negativen Brustkrebs (TNBC) ist sein Ziel. Anstatt einen Infektionserreger zu bekämpfen, verwendet der Impfstoff eine im Labor hergestellte (rekombinante) Version von α-Lactalbumin, um das Immunsystem sicher mit diesem Protein in Kontakt zu bringen und eine gezielte Immunantwort auszulösen. α-Lactalbumin ist ein Milchprotein, das normalerweise nur in der Spätschwangerschaft und während der Stillzeit aktiv ist und ansonsten im Brustgewebe Erwachsener keine Aktivität aufweist. In über 70 % der TNBC-Tumoren wird α-Lactalbumin jedoch abnormal exprimiert und markiert so Krebszellen, die vom durch den Impfstoff trainierten Immunsystem erkannt werden können.
Dies ist die Grundlage der sogenannten „Hypothese der inaktiven Proteine“, die von Forschern der Cleveland Clinic entwickelt wurde. Manche Proteine erfüllen in der frühen Lebensphase, beispielsweise während des Stillens, wichtige Funktionen und werden dann quasi inaktiviert, sobald sie nicht mehr benötigt werden. Wenn ein Tumor diese inaktivierten Proteine später reaktiviert, stellen sie eine seltene Art von Zielstruktur dar: körpereigene Proteine, die in gesunden Zellen nicht aktiv genutzt werden. Dadurch wird die Wahrscheinlichkeit deutlich verringert, dass ein gegen den Tumor gerichteter Immunangriff auf gesundes Gewebe übergreift und Autoimmunität auslöst.
Obwohl der genaue Grund für die Reaktivierung von α-Lactalbumin durch TNBC weiterhin unklar ist, vermuten Wissenschaftler, dass das Fehlen von Östrogen- und Progesteronrezeptoren bei TNBC hormonelle Signalwege stört, die normalerweise α-Lactalbumin unterdrücken. Dieses Phänomen hat somit ein Zeitfenster der Verwundbarkeit geschaffen, das Impfstoffentwickler gezielt ausnutzen wollen. „Tumore verhalten sich manchmal seltsam“, sagte Dr. Vincent Tuohy, Immunologe am Lerner Research Institute der Cleveland Clinic in den USA und Entwickler des α-Lactalbumin-Impfstoffs. „Die Expression von α-Lactalbumin ist ein Fehler, den TNBC-Tumore begehen, und genau diesen Fehler machen wir uns zunutze.“
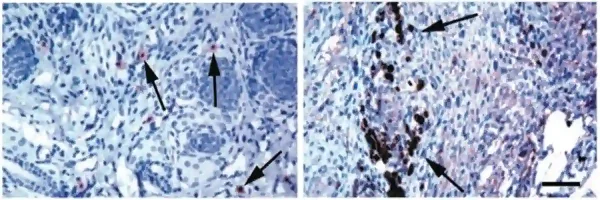
In präklinischen Mausmodellen schützte die Impfung mit α-Lactalbumin vor Brusttumoren, ohne bei nicht-laktierenden Mäusen Entzündungen auszulösen. Im Gegensatz dazu führte die Impfung laktierender Mäuse zu Brustentzündungen und Stillversagen (Abbildung 2). Dieser Zusammenhang entspricht genau den Erwartungen, wenn α-Lactalbumin nur in der Spätschwangerschaft oder während der Stillzeit exprimiert wird. Daher ist der α-Lactalbumin-Impfstoff, sofern zukünftige Studien keine anderen Ergebnisse liefern, für Personen vorgesehen, die weder schwanger werden noch stillen möchten. Wissenschaftler der Cleveland Clinic schrieben: „Die α-Lactalbumin-Impfung könnte Frauen nach der Familienplanung und vor den Wechseljahren, also in einem Alter, in dem Stillen leicht vermieden werden kann und das Brustkrebsrisiko hoch ist, einen sicheren und wirksamen Schutz vor Brustkrebs bieten.“
Abbildung 2. Immunantwort auf die α-Lactalbumin-Impfung in Abhängigkeit vom Laktationsstatus. Die Mikroskop-Aufnahmen zeigen Brustgewebe geimpfter Mäuse. Linke Abbildung: Bei nicht-laktierenden Mäusen patrouillieren nur wenige T-Zellen (Pfeile) im Brustgewebe; Entzündungszeichen fehlen. Rechte Abbildung: Bei laktierenden Mäusen, bei denen α-Lactalbumin natürlicherweise aktiviert ist, löst dieselbe Impfung eine starke Immunreaktion aus, die sich durch die Ansammlung zahlreicher Immunzellen im Brustgewebe (dunkel gefärbte Bereiche) äußert. Quelle: Jaini et al. (2010), Nature Medicine.
α-Lactalbumin-Impfstoff gegen TNBC: Erste klinische Ergebnisse
Der rekombinante α-Lactalbumin-Impfstoff hat die präklinische Phase hinter sich gelassen und befindet sich nun in der frühen klinischen Prüfung am Menschen. In der Phase-1-Studie erhielten die Teilnehmer den mit Zymosan (einem aus Hefe gewonnenen Adjuvans zur Aktivierung der Immunantwort) formulierten rekombinanten α-Lactalbumin-Impfstoff. Die Impfung erfolgte in drei Dosen im Abstand von zwei Wochen nach einem Standard-Dosis-Eskalationsdesign. Um zu beurteilen, ob der Impfstoff das Immunsystem erfolgreich aktiviert hat, maßen die Forscher α-Lactalbumin-spezifische Immunantworten, darunter die T-Zell-Aktivierung, die Zytokin-Produktion und die Antikörperantwort.
Wie bei allen Studien der Phase I am Menschen war das Ziel dieser Phase-1-Studie bewusst begrenzt. Sie war nicht darauf ausgelegt, nachzuweisen, dass der Impfstoff ein Wiederauftreten von Krebs oder die Entstehung neuer Tumore verhindert. Stattdessen sollten zwei grundlegende Fragen beantwortet werden:
- Ist der Impfstoff sicher und verträglich?
- Kann er beim Menschen zuverlässig eine Immunantwort gegen α-Lactalbumin auslösen?
Um diese Fragen zu beantworten, wurden 35 Teilnehmer in drei klinischen Gruppen in die Studie aufgenommen:
- Phase Ia umfasste Überlebende von dreifach negativem Brustkrebs (TNBC), die die Standardtherapie abgeschlossen hatten und krebsfrei waren, aber ein hohes Rückfallrisiko aufwiesen.
- Phase Ib umfasste krebsfreie Personen mit einer starken genetischen Prädisposition für TNBC, wie z. B. BRCA-Mutationsträger, die sich einer risikomindernden Operation unterzogen.
- Phase Ic umfasste Patientinnen mit residualem TNBC nach Chemo-Immuntherapie und Operation, die eine adjuvante Immuntherapie erhielten.
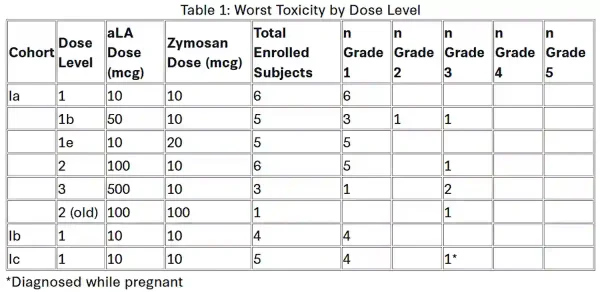
Insgesamt erwies sich der Impfstoff als sicher und gut verträglich. Etwa 74 % der Teilnehmenden entwickelten eine messbare Immunantwort auf α-Lactalbumin. Die meisten Nebenwirkungen waren mild und beschränkten sich auf die Injektionsstelle, wie Rötungen oder Unbehagen. Wie in Dosis-Eskalationsstudien üblich, traten bei höheren Dosen schwerere lokale Reaktionen, wie z. B. Ulzerationen, die eine Drainage erforderten, auf und trugen zur Bestimmung der maximal tolerierten Dosis bei. Dieses Vorgehen ist Standard in frühen klinischen Studien (Abbildung 3). Studienleiter Dr. G. Thomas Budd vom Taussig Cancer Institute der Cleveland Clinic erklärte: „Die Ergebnisse dieser Studie sind vielversprechend, da sie darauf hindeuten, dass der Prüfimpfstoff nicht nur sicher und gut verträglich ist, sondern auch bei über 70 % der Teilnehmenden eine Immunantwort auslösen kann.“
Abbildung 3. Sicherheitsprofil des α-Lactalbumin-Impfstoffs bei verschiedenen Dosierungen in den drei Studienkohorten (Phase Ia bis Ic). Nebenwirkungen wurden von Grad 1 (leicht) bis Grad 5 (lebensbedrohlich oder tödlich) eingeteilt. Die meisten Teilnehmenden zeigten lediglich leichte Reaktionen (Grad 1), typischerweise an der Injektionsstelle. Schwerere Reaktionen der Grade 2–3 (z. B. Ulzerationen, die eine Drainage erforderten) traten selten auf und halfen den Forschenden, die maximal tolerierte Dosis des Impfstoffs zu bestimmen. Quelle: Johnson et al. (2025), Posterpräsentation 4 beim San Antonio Breast Cancer Symposium.
Der Nachweis der Immunogenität allein bedeutet jedoch noch nicht, dass der Impfstoff Krebs verhindert. Er erfüllt vielmehr eine entscheidende Voraussetzung: dass eine α-Lactalbumin-spezifische Immunität in geeigneten Dosen sicher beim Menschen erzeugt werden kann. Dieser Meilenstein ebnet den Weg für die Phase-2-Studie, in der geprüft werden soll, ob diese Immunisierung zu einem tatsächlichen klinischen Nutzen führt.
Ermutigend ist, dass diese Impfstrategie in einem Kontext getestet wird, in dem Krebsimpfstoffe besonders erfolgversprechend sind. Anders als bereits bestehende Tumore hatten neu entstehende Krebszellen kaum Zeit, Mechanismen zur Immunflucht zu entwickeln, wodurch sie anfälliger für die Immunüberwachung sind. Sollten zukünftige Studien zeigen, dass eine gegen α-Lactalbumin gerichtete Immunität das Wiederauftreten von Tumoren verringern oder die Tumorentstehung bei Hochrisikopatienten verhindern kann, würde dies einen grundlegenden Wandel im Umgang mit Krebs bedeuten: nicht mehr als Krankheit, die nach ihrem Ausbruch behandelt werden muss, sondern als biologischer Prozess, der sich eindämmen lässt, bevor er sich manifestiert.
„Es gab eine Zeit, da hieß es, HER2 sei die schlimmste Form von Brustkrebs, die man haben kann. Dann kamen die HER2-gerichteten Therapien auf den Markt, und plötzlich ist einer der schlechtesten Prognosemarker einer der besten“, sagte Larry Norton, MD, medizinischer Direktor des Evelyn H. Lauder Brustzentrums in New York. Er ist von den ersten Studienergebnissen beeindruckt. „Dies könnte die Geschichte des dreifach negativen Brustkrebses werden, wenn das Zielmolekül stimmt.“
Selbst wenn der rekombinante α-Lactalbumin-Impfstoff in Phase-2-Studien keinen klinischen Nutzen zeigen sollte, bleibt die Forschung an sich bedeutsam. Wie Dr. Norton bereits festgestellt hat, verbessern Fortschritte in der Tumorbiologie stetig unsere Fähigkeit, ungewöhnliche Moleküle auf Krebszellen zu identifizieren, die therapeutisch angegriffen werden können. In diesem Sinne ist α-Lactalbumin möglicherweise nicht die einzige Lösung, sondern die erste von mehreren potenziellen Angriffspunkten bei TNBC.