Einführung
1907 betonte der britische Chirurg Dr. Charles Childe in seinem Buch „The Control of a Scourge, Or How Cancer Is Curable“ die Bedeutung der Krebsfrüherkennung. Er postulierte, dass die meisten Krebsarten wirksam behandelt werden könnten, wenn sie frühzeitig erkannt würden. Obwohl seine Arbeit im britischen Gesundheitssystem nur begrenzten Einfluss hatte, inspirierte sie die American Medical Association dazu, regelmäßige Gesundheitschecks zur Krebsfrüherkennung zu fördern und führte in den 1920er Jahren den Begriff „Screening“ in die medizinische Fachsprache ein.
Zu dieser Zeit waren klinische Studien noch nicht weit verbreitet. Die Medizin stützte sich daher stärker auf professionelles Urteilsvermögen und Einzelfallberichte. Da klinische Studien jedoch zum Maßstab für die Entwicklung medizinischer Richtlinien wurden, geriet die Wirksamkeit von Krebsvorsorgeuntersuchungen in den Fokus, was zu einer Neubewertung ihres Nutzens im modernen Gesundheitswesen führte.
beispielsweise eine Metaanalyse von 18 klinischen Studien aus dem Jahr 2023, dass fast alle gängigen Krebsvorsorgeuntersuchungen die Lebenserwartung langfristig nicht verlängern. Diese Metaanalyse, die Daten von über zwei Millionen Patienten über 10 bis 15 Jahre umfasste, ergab, dass nur die Sigmoidoskopie zur Darmkrebsvorsorge die Lebenserwartung signifikant um 110 Tage verlängerte. Im Gegensatz dazu hatten die anderen Standard-Screening-Tests (z. B. Computertomographie bei Lungenkrebs, Koloskopie bei Dickdarmkrebs und Mammographie bei Brustkrebs) keinen Einfluss auf die Lebenserwartung.
Insbesondere die Mammographie steht im Mittelpunkt intensiver Debatten über ihr Nutzen-Risiko-Verhältnis. Dieser Newsletter untersucht die tatsächliche Wirksamkeit und Sicherheit der Mammographie im Brustkrebs-Screening und untersucht mögliche Strategien zur Verbesserung ihres Nutzens.
Argumentierten in Bezug auf die Ergebnisse der Metaanalyse, dass Screenings zwar die allgemeine Lebenserwartung nicht wesentlich verändern, aber einen frühen Krebstod verhindern können. So verlängert ein Krebsscreening die Lebenserwartung zwar nicht von 80 auf 90 Jahre, kann aber einen vorzeitigen Tod mit 65 Jahren verhindern und die erwartete Lebenserwartung von 80 Jahren erreichen. Ob Mammographien wirksam sind oder nicht, hängt daher vom verwendeten Messverfahren ab.
Mammographien sind hilfreich, um Brustkrebs frühzeitig zu erkennen, noch bevor Symptome auftreten. Eine Studie berichtete, dass bei Brustkrebs mit Mammographie-Screening eine 10-Jahres-Überlebensrate von 80 % auftrat, verglichen mit 63 % bei Krebsfällen, die erst bei Symptombeginn erkannt wurden. Das Stadium des Krebses bestimmt oft die erforderliche Behandlungsintensität, wobei fortgeschrittene Stadien aggressivere Therapien erfordern. Untersuchungen haben gezeigt, dass Frauen, die nicht untersucht wurden, im Vergleich zu Frauen, die sich regelmäßigen Screenings unterziehen, mehr als doppelt so häufig intensive Behandlungen wie Chemotherapie und Operationen benötigen. Diese Ergebnisse verdeutlichen, dass Mammographien zwar nicht für alle von Nutzen sein mögen, aber für eine Untergruppe von Frauen mit verstecktem, zugrunde liegendem Brustkrebs einen signifikanten Unterschied machen.
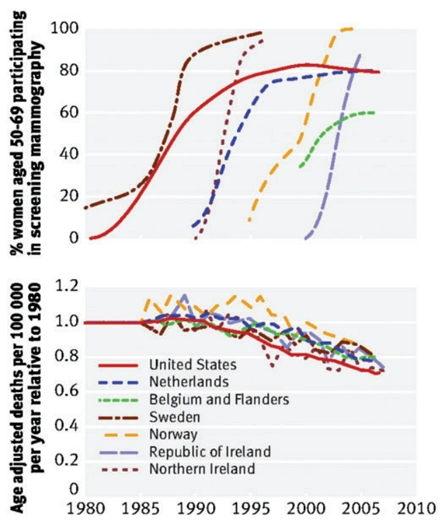
Ein Vorbehalt ist jedoch die hohe Anzahl notwendiger Screenings (NNS), also die Anzahl der Frauen, die untersucht werden müssen, um einen Todesfall zu verhindern. Eine systematische Übersichtsarbeit beziffert die NNS der Mammographie auf 2.449, 1.503 und 1.159 für Frauen im Alter von 40–49, 50–59 und 60–69 Jahren. Somit müssen sich mindestens tausend Frauen einer Mammographie unterziehen, um eine Frau vor Brustkrebs zu bewahren. Dies erklärt auch, warum die Einführung regelmäßiger Mammographie-Screenings nicht mit einer Senkung der Brustkrebsmortalität auf nationaler Ebene korreliert (Abbildung 1). Stattdessen begann der Rückgang der Brustkrebsmortalität länderübergreifend um 1990, zeitgleich mit der Einführung wirksamerer Krebstherapien. Zu diesem Zweck empfiehlt die Schweizerische Ärztekammer das Mammographie-Screening gänzlich einzustellen , da der Nutzen die damit verbundenen Risiken und Schäden nicht rechtfertigt.
Abbildung 1. Die Einführung regelmäßiger Mammographie-Screenings korrelierte nicht mit der nationalen Brustkrebs-Sterblichkeitsrate. Oben: Anteil der Frauen, die in den einzelnen Ländern regelmäßig an Mammographie-Screenings teilnahmen. Unten: Veränderungen der Brustkrebs-Sterblichkeitsraten in den einzelnen Ländern. Quelle: Gøtzscheet (2015), Journal of the Royal Society of Medicine.
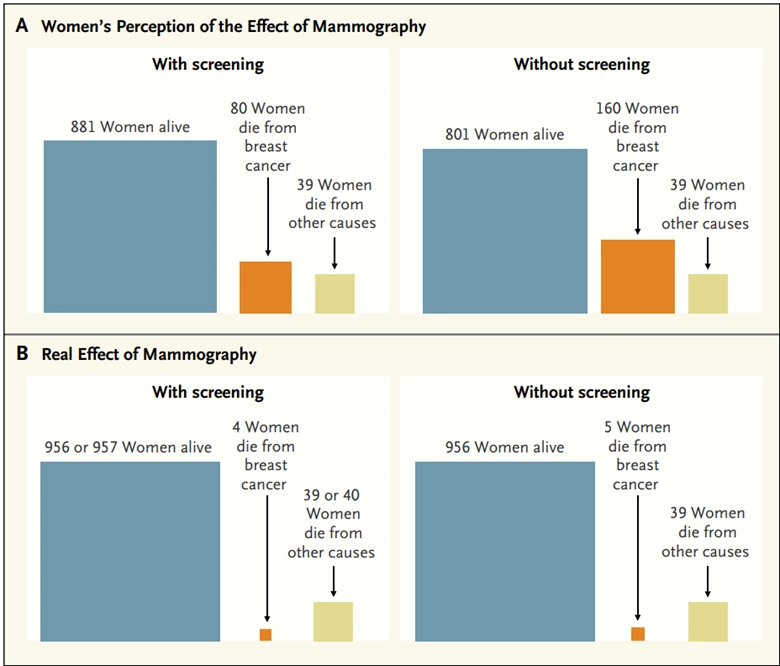
Die Schweizer Ärztekammer zeigte sich zudem beunruhigt darüber, dass die meisten Frauen den Nutzen der Mammographie drastisch überschätzen. Eine in den USA, Großbritannien, Italien und der Schweiz durchgeführte Umfrage ergab, dass rund 70 % der Frauen glaubten, dass das Mammographie-Screening die Brustkrebssterblichkeit um mindestens 50 % senkt und 10 Todesfälle pro 1.000 Frauen verhindert. Die tatsächliche NNS-Kennzahl deutet jedoch eindeutig auf etwas anderes hin (Abbildung 2). Bemerkenswerterweise wurde in der Umfrage nicht untersucht, wie gut sich die Frauen der möglichen negativen Auswirkungen der Mammographie, wie Fehldiagnosen und Strahlenbelastung, bewusst sind. Dies deutet darauf hin, dass Frauen möglicherweise unrealistische Erwartungen an das Nutzen-Risiko-Verhältnis des Mammographie-Screenings haben.
Abbildung 2. Wahrnehmung des Nutzens des Mammographie-Screenings für die Brustkrebssterblichkeit durch Frauen im Vergleich zum tatsächlichen Nutzen. Quelle: Biller- Andorno und Jüni (2014), New England Journal of Medicine.
Tatsächlich ist die Genauigkeit der Mammographie nicht perfekt und liegt bei etwa 85-90 %. Das erscheint zwar hoch, bedeutet aber auch, dass die Rate falsch positiver Ergebnisse (d. h. die Erkennung von Krebs, obwohl keiner vorhanden ist) bei etwa 10 % liegt. Würden alle Frauen einer Mammographie unterzogen, würde dies dazu führen, dass 10 % der Bevölkerung fälschlicherweise mit nicht vorhandenem Brustkrebs diagnostiziert würden. Bei 10 Jahren jährlicher Mammographie-Screenings steigt die Wahrscheinlichkeit falsch positiver Ergebnisse auf 50-60%.
Solche Fehldiagnosen können zu unnötigen Angst und führen zu Medizinische Eingriffe, die nicht nur sinnlos sein können, sondern auch zusätzliche Risiken und Kosten bergen. Beispielsweise könnten bei einer Gruppe von 1.000 Frauen im Alter von 50 Jahren, die sich zehn Jahre lang jährlich einer Mammographie unterziehen, zwischen 0,3 und 3,2 Frauen vor dem Tod durch Brustkrebs bewahrt werden. Diese Praxis führt jedoch dazu, dass 490–670 Frauen mindestens eine falsch positive Diagnose erhalten, wobei 70–100 bzw. 3–14 von ihnen unnötigen Biopsien und Behandlungen (z. B. Bestrahlung, Operation oder Chemotherapie) unterzogen werden. Infolgedessen belaufen sich die wirtschaftlichen Kosten des regelmäßigen Mammographie-Screenings auf geschätzte Kosten Milliarden von Dollar pro Jahr allein in den USA.
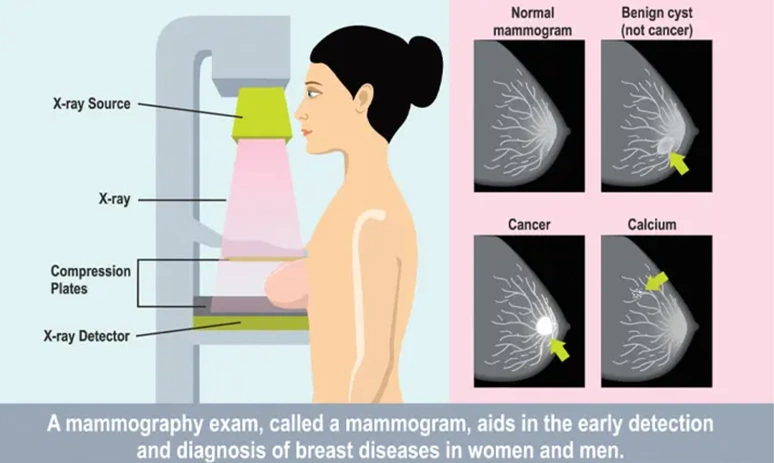
der Mammographie werden geringe Dosen ionisierender Strahlung in Form von Röntgenstrahlen eingesetzt, um detaillierte Bilder des Brustgewebes zu erzeugen (Abbildung 3). Diese Bilder können dann auf Anzeichen von Krebs, wie Knoten oder Mikroverkalkungen, untersucht werden. Übermäßige Strahlenbelastung kann jedoch DNA-Schäden und Krebs verursachen. Strahlenbedingter Krebs ist daher ebenfalls eine kleine, aber mögliches Risiko einer Mammographie. Dieses Risiko ist besonders besorgniserregend für Personen mit genetischen Prädispositionen, die die DNA-Reparaturaktivität beeinträchtigen. Bei Frauen ab 40 Jahren schätzten Untersuchungen, dass durch die Mammographie für jedes durch Strahlenbelastung verlorene Leben 36,5 Leben gerettet werden.
Samuel Epstein, MD, gehörte zu den ersten Ärzten, die in den 1990er Jahren die Risiken des Mammographie-Screenings öffentlich hinterfragten. Dr. Epstein betonte, dass das Standardverfahren, jährlich vier Mammographien pro Brust durchzuführen, Frauen einer Strahlendosis von etwa 1 Rad (absorbierte Strahlendosis) aussetzt, was ausreichen kann, um das Brustkrebsrisiko um 0,8 % zu erhöhen. Diese Belastung ist zudem 1.000-mal höher als die Strahlung einer einzigen Röntgenaufnahme des Brustkorbs. Insbesondere das Massenscreening mit Röntgenaufnahmen des Brustkorbs zur Früherkennung von Lungenkrebs und Tuberkulose wurde in vielen Ländern eingestellt, da es tendenziell mehr Krebs verursachte als erkannte.
Abbildung 3. So funktioniert die Mammographie. Quelle: Mount Elizabeth Hospital (2021).
Auch die Mammographie ist keine schmerzfreie Angelegenheit. Um präzise Bilder zu erhalten, muss das Mammographiegerät die Brust komprimieren. Systematic Untersuchungen ergaben, dass 77 % bzw. 28 % der Frauen während der Mammographie Schmerzen und erhebliche Schmerzen hatten. Fast 50 % der Frauen wurden aufgrund der Schmerzen von der Teilnahme am anschließenden Mammographie-Screening abgehalten. Dr. Epstein warnte außerdem, dass eine solche Kompression kleine Blutgefäße in oder um einen unentdeckten Brustkrebs platzen lassen könnte. Dies könnte möglicherweise die Ausbreitung von Krebszellen in den Blutkreislauf auslösen, was das Risiko für Metastasen erhöhen kann.
Trotz der Wirksamkeit und Sicherheitsbedenken der Mammographie ist es nicht praktikabel, diese Technologie abzuschaffen . Das Mammographie-Screening kommt nach wie vor einer kleinen Gruppe von Frauen mit Brustkrebsrisiko zugute und ist für die Diagnose von Brustkrebs von entscheidender Bedeutung. Daher sollten sich die Forschungsanstrengungen auf die Erforschung individualisierter Screening-Ansätze, ergänzender Methoden und sogar neuer Technologien als Ersatz für die Mammographie konzentrieren.
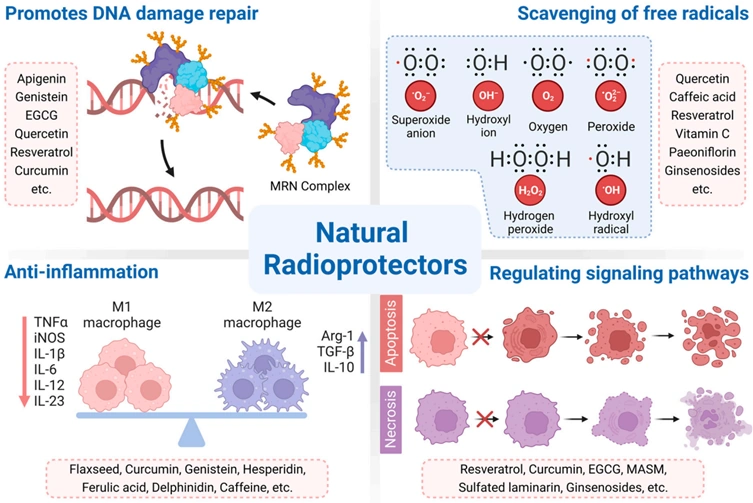
Individualisierten Screening sollten nur diejenigen Personen untersucht werden, bei denen ein Risiko für Brustkrebs besteht, z. B. aufgrund von Brustkrebs in der Familie, einer persönlichen Strahlentherapie des Brustkorbs oder bestimmten genetischen Risikofaktoren. Komplementärmedizin, die auf die Minimierung von oxidativem Stress und DNA-Schäden durch ionisierende Strahlung oder Röntgenstrahlen abzielt, wäre ebenfalls hilfreich. Das Pfeifer-Protokoll ist ein bemerkenswertes Beispiel dafür, da es pflanzliche Verbindungen mit robusten bioaktiven Wirkungen nutzt, darunter krebshemmende, antioxidative und DNA-reparierende Eigenschaften. Ein umfassender Übersichtsartikel aus dem Jahr 2023 unterstrich die strahlenschützenden Mechanismen mehrerer pflanzlicher Verbindungen (Abbildung 3), von denen die meisten auch im Pfeifer-Protokoll enthalten sind, wie z. B.:
- Resveratrol, ein Polyphenol aus Trauben und Beeren, schützt Zellen nachweislich vor strahlenbedingten DNA-Schäden. Unter oxidativem Stress wandert das Enzym Tyrosyl-tRNA-Synthetase ( TyrRS ) in den Zellkern, um die DNA zu schützen. Resveratrol kann die Aktivität von TyrRS steigern, sodass es schneller in den Zellkern gelangen und DNA-Schäden wirksamer verhindern kann.
- Curcumin, ein Polyphenol aus Kurkuma, kann die Reparatur von Doppelstrangbrüchen in der DNA erleichtern, die als die schlimmsten gelten. Form von DNA-Schäden. Curcumin erreicht dies durch vielfältige Mechanismen wie die Aktivierung von DNA-Reparaturenzymen und die Verringerung von oxidativem Stress und Entzündungen.
- Quercetin, ein Flavonoid, das in Obst und Gemüse reichlich vorhanden ist, hat sich auch als Unterdrücken Sie DNA-Doppelstrangbrüche in Zellen, die Röntgenstrahlen ausgesetzt sind, indem Sie die Expression von Bmi-1 hochregulieren, einem unverzichtbaren Protein, das an der Wundheilung und DNA-Reparatur beteiligt ist.
Abbildung 4. Eine Zusammenfassung der radioprotektiven Mechanismen bestimmter Pflanzenstoffe, einschließlich der Reparatur von DNA-Schäden, der Beseitigung freier Radikale zur Reduzierung von oxidativem Stress, der Verringerung von Entzündungen und der Regulierung der Zellsignalisierung. Quelle: Zhang et al. (2023), Cancers.
Alternativ können auch andere Methoden zur Früherkennung von Brustkrebs in Betracht gezogen werden, wie etwa Thermografie, Magnetresonanztomografie (MRT) und Flüssigbiopsie. Diese Methoden sind jedoch aus verschiedenen Gründen, wie mangelnder Genauigkeit, hohen Kosten und nicht standardisierten Protokollen, weniger verbreitet als die Mammografie und erfordern daher weitere Entwicklungen.
- Die Thermografie nutzt Infrarotkameras, um Wärmemuster und Blutfluss im Brustgewebe zu erfassen. Ziel ist es, abnormale Temperaturschwankungen zu identifizieren, die auf Krebs hindeuten. Die Food and Drug Administration (FDA) hat die Thermografie als ergänzendes Verfahren zugelassen, das heißt, sie sollte nur als Ergänzung zu einer primären Methode zur Brustkrebserkennung eingesetzt werden. Es gibt jedoch Bemühungen, die Genauigkeit der Thermographie, die gegenüber der die Mammographie mehrere Vorteile bietet, wie beispielsweise geringere Kosten und keine Strahlung.
- Zweitens nutzt die MRT Magnetfelder und Radiowellen, um detaillierte Bilder des Brustgewebes zu erstellen und so Anomalien oder Tumore zu identifizieren. Allerdings ist sie im Vergleich zur Mammographie mit Herausforderungen wie hohen Kosten und eingeschränkter Verfügbarkeit verbunden. Dennoch ist die MRT besonders vorteilhaft bei der Brustkrebserkennung bei jüngeren Frauen mit dichtem Brustgewebe oder bei Frauen mit Brustimplantaten, bei denen die Genauigkeit der Mammographie abnimmt. Weitere Vorteile der MRT sind die fehlende Strahlenbelastung und der Wegfall körperlicher Kompression.
- Funktioniert die Flüssigbiopsie zur Brustkrebserkennung durch die Analyse von Blutproben auf zirkulierende Tumorzellen oder Krebszell-DNA. Diese Methode bietet zwar eine nicht-invasive Möglichkeit zur Krebserkennung und -überwachung, weist jedoch Einschränkungen auf, darunter eine geringere Genauigkeit bei lokalisierten Tumoren und die fehlende Standardisierung der Probenentnahme und -analyse. Ungeachtet dessen laufen Initiativen zur Entwicklung automatisierter Flüssigbiopsieanalysen mit verbesserter Genauigkeit.
Insgesamt ist die Fähigkeit der Mammographie, Brustkrebs im Frühstadium zu erkennen, zweifellos von entscheidender Bedeutung. Bedenken hinsichtlich Genauigkeit, Unbehagen und Strahlenbelastung erfordern jedoch differenziertere Ansätze. Dazu gehören personalisierte Screening-Protokolle und die Implementierung ergänzender Strategien zur Minderung potenzieller negativer Auswirkungen der Mammographie. Darüber hinaus besteht dringender Bedarf an der Entwicklung vielversprechender alternativer Erkennungsmethoden. Ziel ist es, die Mammographie als Standardmethode zur Brustkrebserkennung zu überwinden und so die medizinische Praxis in diesem Bereich zu verbessern.